ضدانعقادها در همودیالیز در بیماران مبتلا به نارسایی حاد کلیه یا بیماری کلیوی مرحله نهایی
مقدمه:
همودیالیز (HD) و درمانهای جایگزین مداوم کلیه (CKRT) نیاز به دسترسی به خون دارند. خون هنگام عبور از مدارهای HD و CKRT در تماس با سطوحی با میزان ترومبوژنیک مختلف قرار میگیرد. در صورت لخته شدن خون در مدار، تقریباً ۱۸۰ تا ۲۰۰ میلیلیتر خون ممکن است از بین برود، زیرا امکان بازگرداندن آن به بیمار وجود ندارد. علاوه بر از دست رفتن خون، لخته شدن در فیبرهای مویرگی صافی باعث کاهش میزان حذف مواد زائد و کاهش طول عمر صافی میشود. بنابراین، نوعی از ضدانعقاد (مانند هپارین غیرفرکشنه [UFH]) معمولاً در زمان دیالیز تجویز میشود تا از لخته شدن در مدار خونی جلوگیری شود.
نوع داروی ضدانعقاد مورد استفاده در همودیالیز متناوب، در مناطق مختلف جهان، کشورهای گوناگون و حتی در مراکز دیالیز یک کشور متفاوت است. با وجود گزینههای جایگزین مختلف، هپارین همچنان رایجترین داروی ضدانعقاد مورد استفاده است. در ایالات متحده، عمدتاً از هپارین غیرفرکشنه (Unfractionated Heparin) استفاده میشود، در حالی که در اتحادیه اروپا، هپارین با وزن مولکولی پایین (LMWH) به عنوان گزینهی منتخب، توصیه شده است.
تعداد کمی از مراکز دیالیز از سیترات تریسدیم (Trisodium Citrate) برای ضدانعقاد مدار خون استفاده میکنند. همچنین، در شرایط خاص، داروهای مهارکننده مستقیم ترومبین مانند آرگاتروبان (Argatroban)، هپارینوئیدها (داناپاروئید، فونداپارینوکس)، پروستانوئیدها و نافاموستات مالئات (Nafamostat Maleate) میتوانند به عنوان جایگزینهای ضدانعقادی مورد استفاده قرار گیرند این مقاله به بررسی ضدانعقاد در همودیالیز متناوب در بیماران مبتلا به نارسایی حاد کلیه یا بیماری کلیوی مرحله نهایی میپردازد.
اهمیت آنتی کواگولاسیون در دیالیز
هنگامی که خون با سطوح خارجی مانند لولههای خونی و صافی تماس پیدا میکند، مکانیسم لخته شدن آن فعال میشود. این مکانیسم از طریق چسبیدن و تجمع پلاکتها روی این سطوح خارجی آغاز میشود. پلاکتها در اثر تماس با سطح خارجی آسیب میبینند و در نتیجه، فاکتورهایی آزاد میکنند که باعث چسبیدن پلاکتها و شروع فرآیند لخته شدن میشود. در ادامه، مسیر لخته شدن خارجی ممکن است به تشکیل ترومبوز شدید و لخته شدن مدار خارجبدنی (دیالیز) منجر شود.
توجه:
دو مسیر اصلی برای لخته شدن وجود دارد:
• مسیر درونی: زمانی فعال میشود که پارگی در عروق بدن رخ دهد (مانند خونریزی گوارشی یا آنوریسم).
• مسیر بیرونی: در اثر تماس خون با هوا یا مواد خارجی فعال میشود.
هپارین
هپارین داروی ضدانعقاد اصلی در دیالیز محسوب میشود. این دارو با آنتیترومبین III در گردش خون متصل شده و سپس با آنزیمهای مختلف فاکتورهای انعقادی ترکیب میشود و آنها را در سطح غشای پلاکتی غیرفعال میکند. هپارین تأثیر کمی بر تعامل پلاکتها با سطح دارد.
• نیمهعمر هپارین بین 30 تا 120 دقیقه است.
• نیمهعمر هپارین در بیماران دیالیزی بهطور میانگین 50 دقیقه است، اما بین 30 دقیقه تا 2 ساعت متغیر میباشد.
• اثرات هپارین را میتوان با استفاده از پروتامين سولفات معکوس کرد.
• پروتامين سولفات همچنین در "هپارینسازی منطقهای" کاربرد دارد.
• PTT یک روش عینی برای پایش اثربخشی هپارین است
• INR/PT برای پایش عینی تأثیرات ضدانعقادی وارفارین (Coumadin) استفاده میشود.
عوارض جانبی شایع هپارین شامل موارد زیر است:
• خارش (Pruritus)
• واکنشهای آلرژیک
• ریزش مو (Alopecia)
• پوکی استخوان
• افزایش چربی خون (Hyperlipidemia)
• ترومبوسیتوپنی (Thrombocytopenia)
• خونریزی بیش از حد
برای اطلاعات بیشتر در این مورد به مقاله نواع هپارین و پروتکل های ضد انعقاد در دیالیز مراجعه کنید.
ارزیابی خطر خونریزی
استفاده از ضدانعقاد در همودیالیز متناوب (HD) به دلیل تمایل زیاد به لخته شدن در مدار خارج بدنی، رایج است. با این حال، تصمیم برای تجویز ضدانعقاد با ارزیابی خطر خونریزی بیمار آغاز میشود.
بیمارانی که تحت HD قرار دارند، معمولاً مستعد تشکیل لخته هستند، بهویژه پس از یک عمل جراحی و در معرض خطر افزایشیافته لخته شدن در مدار دیالیز قرار دارند. با این حال، در برخی گروههای بیماران، خطر خونریزی بیشتر از خطر لخته شدن است.
این گروهها شامل:
• ترومبوسیتوپنی شدید(تعداد پلاکت کمتر از ۲۰,۰۰۰ در هر میکرولیتر)
• وجود خونریزی فعال از دستگاه گوارش، خونریزی داخل شکمی، خونریزی گسترده از زخمهای جراحی، یا خونریزی شدید از کاتترهای شریانی یا وریدی در زمان دیالیز
• عمل جراحی بزرگ(بهویژه جراحیهای داخل چشمی و ستون فقرات) در ۷۲ ساعت گذشته
• خونریزی فعال داخل جمجمهای یا خارجسختشامهای
• استفاده از داروهای ضدانعقاد سیستمیک
• پریکاردیت اورمیک
• کمبود فاکتور انعقادی VII یا VIII
بیمارانی که شرایط فوق را ندارند، در دسته بیماران با خطر استاندارد قرار میگیرند و مطابق با دستورالعملهای زیر درمان میشوند.
بیمارانی که کمبود فاکتورهای انعقادی IX، XI و XII دارند، در معرض خطر بالای خونریزی با استفاده از ضدانعقاد در HD معمولی سرپایی در نظر گرفته نمیشوند. این امر به این دلیل است که لخته شدن در مدار همودیالیز عمدتاً توسط فاکتور VII، همراه با فعالسازی پلاکتها و لکوسیتها ایجاد میشود. با این حال، بیماران مبتلا به هموفیلی A (کمبود فاکتور VIII) ممکن است پس از خارج کردن سوزن از محل دسترسی شریانی-وریدی دچار خونریزی طولانی شوند و نیاز به تزریق فاکتور VIII نوترکیب قبل از برداشتن سوزن داشته باشند. بنابراین، کمبود سایر فاکتورهای انعقادی بهجز فاکتورهای VII و VIII، خطر خونریزی بیشتری در طول HD ایجاد نمیکند.
استفاده از داروهای ضدپلاکتی بهتنهایی بهعنوان یک عامل خطر خونریزی در بیماران تحت HD در نظر گرفته نمیشود. علاوه بر این، ترکیب داروهای ضدپلاکتی مانند آسپرین و کلوپیدوگرل در دوزهای استاندارد، خطر خونریزی در محل سوزن را افزایش نمیدهد؛ اما یک مطالعه نشان داده است که ترکیب این داروها در دوزهای بالاتر ممکن است خونریزی در محل سوزن را در بیمارانی که از گرافت شریانی-وریدی استفاده میکنند، افزایش دهد.
بیمارانی که تحت جراحی بزرگ قرار گرفتهاند، معمولاً بلافاصله پس از عمل جراحی مستعد تشکیل لخته هستند. خطر خونریزی در این بیماران، با گذر زمان کاهش مییابد و پس از ۷۲ ساعت از عمل جراحی، خطر خونریزی آنها در مقایسه با بیماران با خطر استاندارد، بیشتر نیست.
رویکرد ضدانعقادی برای بیماران همودیالیزی با ریسک استاندارد
بیماران با ریسک استاندارد
بیمارانی که در گروه ریسک استاندارد برای ضدانعقاد قرار دارند، اکثریت جمعیت بیماران دیالیزی را تشکیل میدهند. استفاده از ضدانعقاد در سراسر جهان متفاوت است. هر دو روش استفاده از هپارین غیرفرکشنه (UFH) و هپارین با وزن مولکولی پایین (LMWH) مؤثر هستند، پروفایل ایمنی مشابهی دارند و استراتژیهای قابل قبولی محسوب میشوند. بنابراین، در بیماران با ریسک استاندارد، یکی از دو روش زیر را به کار میبریم:
۱. استفاده از هپارین غیرفرکشنه (UFH)
بهترین روش برای تجویز دوز اولیه هپارین( 2000 واحد)، تزریق آن از طریق لوله دسترسی وریدی بیمار و شستشو با محلول سالین است (بهجای تزریق آن به لاین خون شریانی ). تزریق هپارین به لاین خون شریانی باعث میشود که خون ورودی بدون هپارین ابتدا از صافی عبور کند، قبل از زمانی که دوز اولیه فرصت پیدا کند که از مدار خارجبدنی عبور کرده و خون را در بدن ضدانعقاد کند. قبل از شروع دیالیز،دوز اولیه هپارین را به دسترسی وریدی تزریق کنید، ۳ تا ۵ دقیقه صبر کنید تا هپارین بهطور یکنواخت در بدن، پخش شود. سپس تزریق مداوم هپارین را به لاین خون شریانی آغاز کنید (مثلاً با سرعت ۱۲۰۰ واحد در ساعت).
نکته :
برخی مراکز یک دوز اولیه بالا (75–100 واحد به ازای هر کیلوگرم وزن بدن) تجویز کرده و سپس تزریق مداوم 500 تا 750 واحد در ساعت انجام میدهند.( هندبوک داگرداس 2015)
در بسیاری از واحدهای دیالیز، از UFH هپارین برای ضدانعقاد طی جلسات همودیالیز (HD) استفاده میشود. روش تجویز آن به این صورت است:
• ابتدا یک دوز بولوس ۲۰۰۰ واحدی در آغاز دیالیز تزریق میشود.
• سپس، انفوزیون مداوم با دوز ۵۰۰ واحد در ساعت انجام میشود.
• این انفوزیون معمولاً ۶۰ دقیقه قبل از پایان دیالیز متوقف میشود، اما بسته به وضعیت لختهزایی بیمار، ممکن است زودتر متوقف گردد.
• در صورت مشاهده لخته، تزریق ۳۰ دقیقه قبل از پایان دیالیز متوقف میشود.
• در بیمارانی که از کاتتر وریدی استفاده میکنند، تزریق هپارین معمولاً تا پایان دیالیز ادامه مییابد.
نکته:
در برخی از مراکز اروپایی، دوز بولوس اولیه ۱۰۰۰ واحد (بهجای ۲۰۰۰ واحد) تجویز میشود.
روش جایگزین بر اساس وزن بیمار:
• بیماران کمتر از ۵۰ کیلوگرم → ۵۰۰ واحد UFH
• بیماران ۵۰ تا ۱۰۰ کیلوگرم → ۱۰۰۰ واحد UFH
• بیماران بیش از ۱۰۰ کیلوگرم → ۲۰۰۰ واحد UFH
روشهای دیگر تجویز UFH (کمتر توصیه میشود):
• تزریق بولوس بدون انفوزیون مداوم
• انفوزیون مداوم بدون تزریق بولوس
• تزریق دو مرحلهای (یک بار در شروع و یک بار در میانه دیالیز) بدون انفوزیون مداوم
• تزریق بولوس اولیه همراه با کاهش تدریجی سرعت انفوزیون
۲. استفاده از هپارین با وزن مولکولی پایین (LMWH)
LMWH بیشتر در اروپای غربی، بخشهایی از آسیا و استرالیا برای ضدانعقاد در همودیالیز استفاده میشود. دوز LMWH بسته به نوع دارو و طول جلسه دیالیز متغیر است. مثال:
• تینزاپارین (Tinzaparin): با کوتاهترین نیمهعمر، بهصورت بولوس ۲۵۰۰ واحد ضد-Xa برای یک جلسه ۴ ساعته دیالیز تجویز میشود.
ش انوکساپارین (Enoxaparin): با طولانیترین نیمهعمر، بهصورت ۲۰ میلیگرم برای یک جلسه ۴ ساعته دیالیز تجویز میشود.
در بیماران تحت درمان با LMWH کوتاهاثر مانند تینزاپارین که جلسات دیالیز آنها بیش از ۴ ساعت طول میکشد، ممکن است نیاز به تزریق مجدد (با همان دوز یا دوز کمتر) باشد. با این حال، برخی مراکز گزارش دادهاند که یک دوز بولوس برای دیالیز تا ۸ ساعت کافی است.
نحوه تجویز LMWH:
• تزریق در شاخه شریانی صافی انجام میشود، اما ممکن است بخشی از دارو در صافی از بین برود.
• برای کاهش این اتلاف، تزریق بولوس LMWH پس از ۲ تا ۳ دقیقه از شروع دیالیز انجام میشود.
اصلاحات در صورت مشاهده خونریزی یا لخته در جلسه دیالیز
اگر لخته در نیمه اول دیالیز مشاهده شد:
• دوز بولوس UFH را ۵۰۰ واحد افزایش میدهیم (تا حداکثر ۴۰۰۰ واحد در هر جلسه).
اگر لخته در نیمه دوم دیالیز مشاهده شد:
• سرعت انفوزیون UFH را ۱۰۰ واحد در ساعت افزایش میدهیم (تا حداکثر ۱۰۰۰ واحد در ساعت).
• در صورت لخته شدن فیلتر علیرغم تنظیمات ضدانعقادی مناسب، بیمار باید از نظر وجود استنوز در مسیر ورود یا خروج خون دیالیز بررسی شود.
اگر خونریزی از محل سوزن بیش از ۷ دقیقه طول بکشد:
• زمان توقف انفوزیون UFH را ۱۰ دقیقه افزایش میدهیم (معمولاً ۶۰ دقیقه قبل از پایان دیالیز متوقف میشود).
• در بیماران تحت LMWH که دچار خونریزی طولانیمدت میشوند، دوز بولوس جلسه بعدی کاهش مییابد.
• تمام بیمارانی که دچار خونریزی طولانیمدت از مسیر دیالیز میشوند، باید از نظر مشکلات عروقی (مانند استنوز و ترومبوز) بررسی شوند.
• بیماران دیالیزی طولانیمدت ممکن است گهگاه دچار لخته شوند که لزوماً نیاز به تغییر دوز هپارین ندارد،
زیرا:
-
ممکن است لخته شدن به دلیل کاهش سرعت پمپ باشد.
-
ممکن است ناشی از توقفهای مکرر پمپ خون در آن روز باشد.
-
مشکل در کانولاسیون دسترسی ممکن است مسیر انعقادی را فعال کند.
-
حذف بیش از حد مایع ممکن است منجر به افزایش هماتوکریت و در نتیجه چسبندگی بیشتر خون شود.
ریسک فیبریلاسیون دهلیزی و سکته در بیماران همودیالیزی
بیماران تحت درمان همودیالیز (НD) در معرض خطر بیشتری برای توسعه فیبریلاسیون دهلیزی و سکته مغزی هستند. به همین دلیل، تعداد فزایندهای از بیماران با آنتیکوآگولانتهای خوراکی درمان میشوند، از جمله آنتاگونیستهای ویتامین K (وارفارین)، آنتاگونیستهای ضد-Xa (آپیکسابان) و بهتازگی، آنتیبادیهای مونوکلونال ضد-X1 (osocimab/xisomab ) بیمارانی که وارفارین را بهعنوان آنتیکوآگولانت برای دریچههای قلب مصنوعی فلزی تجویز میکنند و هدف نسبت نرمال بینالمللی آنها 3.5 تا 4.5 است، معمولاً به آنتیکوآگولاسیون اضافی برای همودیالیز نیاز ندارند، در حالی که افرادی که به دلیل فیبریلاسیون دهلیزی تحت درمان قرار دارند، اغلب به آنتیکوآگولاسیون نیاز دارند. با این حال، دوز آنتیکوآگولانت سیستمیک انتخابشده باید با کاهش دوز بارگذاری برای UFH و LMWHs حداقل شود.
بیماران با ریسک بالای خونریزی
هیچ روش استانداردی برای جلوگیری از لخته شدن مدار همودیالیز (HD) در بیماران با ریسک بالای خونریزی وجود ندارد. پروتکلها در مؤسسات و کشورهای مختلف متفاوت هستند. دو روشی که در مؤسسات اروپا استفاده میشود، به شرح زیر است:
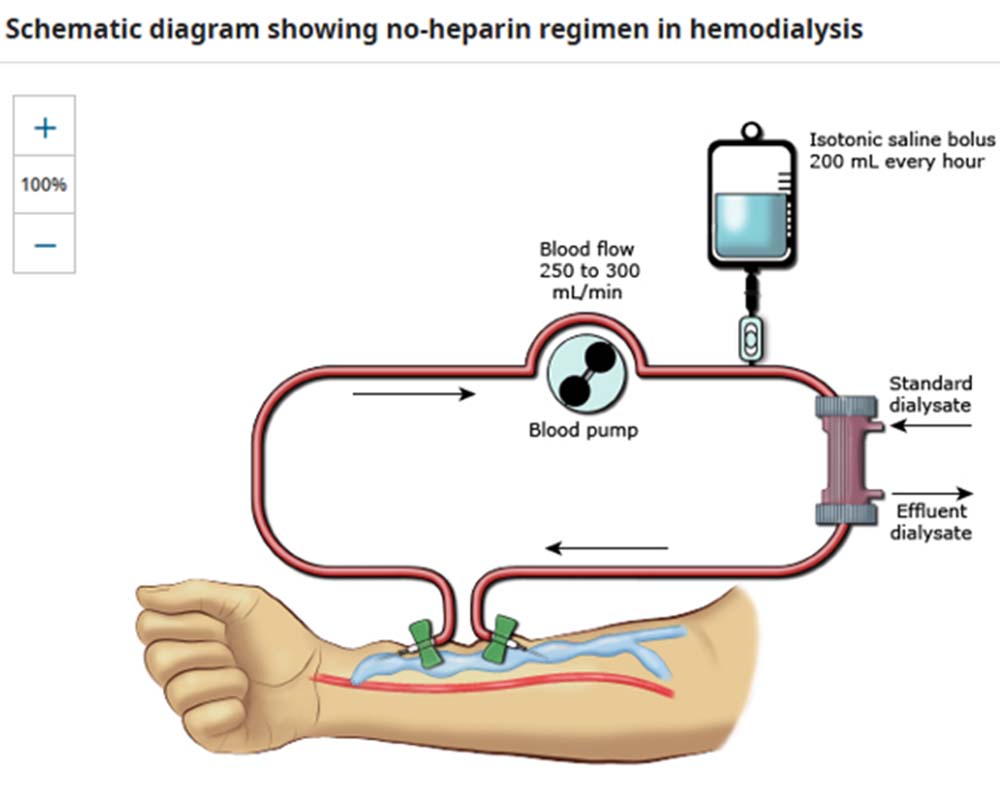
۱. روش بدون هپارین:
در این روش، مدار همودیالیز قبل از ورود بیمار فقط با سالین ایزوتونیک آمادهسازی میشود. سپس، در طول جلسه همودیالیز، شاخه شریانی (قبل از دیالیز) مدار هر ساعت با ۲۰۰ میلیلیتر سالین ایزوتونیک شستوشو داده میشود. مقدار اضافی سالین شستوشو در اهداف اولترافیلتراسیون درمان در نظر گرفته میشود تا از بروز هیپرولمی جلوگیری شود.
نکات مهم:
ن پرستاران باید به هشدارهای فشار شریانی و وریدی توجه ویژه داشته باشند و مدار دیالیز و تلههای حباب را برای شناسایی لختهها بررسی کنند.
• این روش باعث کاهش غلظت خون و شستوشوی رشتههای فیبرین از صافی میشود.
نقطه ضعف:
نیاز به نظارت نزدیکتر پرسنل بر بیمار و افزایش میزان اولترافیلتراسیون برای دفع سدیم و مایع اضافی است.
۲. شستوشو با محلول هپارینه یا استفاده از صافی با پوشش هپارین
در این روش، محلول سالین هپارینه تهیه شده با ۱۰,۰۰۰ تا ۲۰,۰۰۰ واحد هپارین در ۱۰۰۰ تا ۲۰۰۰ میلیلیتر سالین ایزوتونیک، قبل از ورود بیمار به مدار همودیالیز تزریق میشود. سپس این محلول با سالین ایزوتونیک شستوشو داده شده و قبل از اتصال بیمار، هپارین حذف میشود. نکات مهم:
• میزان اتصال هپارین به صافی به ترکیب سطح و بار الکتریکی آن بستگی دارد.
• صافی های پوشش دادهشده با هپارین نیز در بازار موجود هستند، اما مزیت مشخصی نسبت به سایر روشهای بدون ضدانعقاد نشان ندادهاند.
• مطالعات نشان دادهاند که صافی های هپارینه همراه با دیالیزات حاوی سیترات و بدون ضدانعقاد سیستمیک، نسبت به صافی های هپارینه همراه با هپارین سیستمیک، باعث افزایش ایجاد لخته و تولید ترومبین میشوند.
۳. همودیافیلتراسیون پری دیلوشن(Predilution Hemodiafiltration)
در برخی کشورها، همودیافیلتراسیون پیش تزریقی، گزینهای مناسب است که مشابه روش تزریق مداوم سالین عمل میکند. مطالعات نشان دادهاند که ترکیب این روش با دیالیزات حاوی سیترات در بیش از ۹۰٪ موارد موفقیتآمیز بوده است. با این حال، این امر ممکن است به سازگاری صافی با خون بستگی داشته باشد.
بازگشت به پروتکلهای هپارینه
بیشتر بیماران با ریسک بالای خونریزی پس از کاهش خطر خونریزی (مثلاً چند روز پس از تثبیت وضعیت بیمار پس از یک حادثه خونریزی یا جراحی) به پروتکلهای مبتنی بر هپارین بازمیگردند.
بیماران با ترومبوز مکرر فیلتر
بیمارانی که در معرض خطر استاندارد خونریزی قرار دارند و دچار ترومبوز مکرر فیلتر میشوند، باید دوز UFH یا LMWH آنها مطابق با توضیحات بالا تنظیم شود.
**بیمارانی که در معرض خطر بالای خونریزی هستند و با روش بدون هپارین درمان میشوند و همچنان دچار ترومبوز مکرر فیلتر میشوند، **بسته به امکانات محلی، میتوان اقدامات زیر را انجام داد:
• افزایش سرعت جریان خون و استفاده از سوزن با گیج بزرگتر، در صورتی که هنوز این گزینهها به حداکثر مقدار خود نرسیده باشند. در کشورهایی که همودیافیلتراسیون روزانه (HDF) در دسترس است، تغییر به HDF کوتاهمدت روزانه با حجم بالای مایع پیشتزریق (بیش از 40 لیتر) ممکن است گزینهای مناسب باشد.
• افزایش دفعات شستوشوی سالین (مثلاً هر 30 دقیقه به جای هر ساعت) مانند روشی که در بیماران با خطر بالای خونریزی در روش بدون هپارین استفاده میشود.
بیمارانی که به این مداخلات پاسخ نمیدهند و همچنان دچار ترومبوز مکرر میشوند، میتوانند به روشهای زیر تغییر داده شوند:
1.ضدانعقاد مبتنی بر هپارین:
در این روش، بیمار یک بولوس 1000 واحدی UFH در ابتدای دیالیز دریافت میکند (گاهی به این روش «هپارین محدود» گفته میشود). در صورت ادامه لخته شدن، یک بولوس 1000 واحدی UFH در ابتدای دیالیز داده شده و به دنبال آن، انفوزیون 500 واحد در ساعت UFH انجام میشود که در 60 دقیقه پایانی دیالیز قطع خواهد شد (که به این روش «هپارین مینی» گفته میشود). اگر لازم باشد، روش استاندارد ضدانعقاد نیز قابل استفاده است.
2.دیالیز با محلول سیترات:
اسید سیتریک میتواند جایگزین استات یا بیکربنات در دیالیز شود. دیالیز با سیتریت در مقایسه با روش بدون هپارین باعث کاهش تشکیل لخته میشود، زیرا سیتریت با اتصال به کلسیم یونیزهشده، در مسیر انعقاد اختلال ایجاد میکند. نگرانی اصلی در مورد دیالیز با سیتریت، کاهش احتمالی سطح کلسیم و منیزیم یونیزهشده است. با این حال، در غلظت 2.4 mEq/L از اسید سیتریک، تغییرات ایجاد شده در سطح کلسیم و منیزیم معمولاً جزئی بوده و علائم بالینی ایجاد نمیکنند. این روش معمولاً فقط در واحدهای دیالیز بیمارستانی که امکان پایش سطح کلسیم و منیزیم وجود دارد، استفاده میشود.
3.HDF با حجم بالا و اپوپروستنول
اپوپروستنول یک متابولیت آرشیدونیک است که باعث اتساع عروق و مهار تجمع پلاکتی میشود. نیمهعمر اپوپروستنول در شرایط برونتنی (in vitro) بین سه تا پنج دقیقه است، زیرا توسط عضلات صاف اندوتلیال به سرعت متابولیزه میشود. در روش ضدانعقاد منطقهای با اپوپروستنول، این ماده در لوله شریانی دستگاه دیالیز با سرعت 4 تا 8 نانوگرم بر کیلوگرم در دقیقه تزریق میشود. عوارض جانبی شامل سردرد، سرگیجه و گرگرفتگی صورت است که ناشی از اتساع عروق و افت فشار خون میباشد. برای جلوگیری از افت فشار خون، تزریق اپوپروستنول با دوز 0.5 نانوگرم بر کیلوگرم در دقیقه آغاز شده و سپس هر دو دقیقه یکبار، دوز آن دو برابر میشود تا به حداکثر مقدار 8 نانوگرم بر کیلوگرم در دقیقه برسد.
به دلیل نیمهعمر کوتاه، اپوپروستنول قبل از ورود به گردش خون سیستمیک متابولیزه شده و در نتیجه فقط در منطقه دیالیز به عنوان ضدانعقاد عمل میکند.
اگر بیمار علیرغم تنظیم دوز ضدانعقاد و بررسی وضعیت دسترسی عروقی، همچنان دچار ترومبوز مکرر شود، باید ارزیابیهای هماتولوژیک برای بررسی اختلالات انعقادی مستعدکننده ترومبوز انجام شود. این فرآیند معمولاً نیاز به مشاوره با متخصص هماتولوژی دارد تا نتایج آزمایشات بررسی و برنامه مدیریت مناسب تنظیم شود.
بررسی برای اختلالات مستعدکننده ترومبوز شامل شرایط زیر است:
• ترومبوسایتمی
• افزایش فاکتور VIII
• جهشهای پروترومبین
• جهش فاکتور V لیدن
• آنتیبادیهای آنتیکاردیولیپین
• آنتیبادیهای ضد فاکتور 4 پلاکتی (PF4)
• کاهش مهارکنندههای طبیعی انعقاد خون (آنتیترومبین، پروتئین S و پروتئین C)
بیماران مبتلا به ترومبوسیتوپنی القاشده با هپارین (HIT)
دو نوع ترومبوسیتوپنی القاشده با هپارین (HIT) وجود دارد که فقط یکی از آنها از نظر بالینی اهمیت دارد (نوع ۲) :
•HIT نوع 1:
یک کاهش خفیف، گذرا و خودمحدودشونده در تعداد پلاکتها است که معمولاً در دو روز اول پس از قرار گرفتن در معرض هپارین غیرفرکشنهشده (UFH) رخ میدهد. این وضعیت به نظر میرسد که ناشی از تجمع پلاکتها به صورت غیرایمنی باشد. در مورد HIT نوع ۱، نیازی به تغییر در مدیریت ضدانعقاد مرتبط با دیالیز وجود ندارد.
•HIT نوع 2:
یک وضعیت بالینی مهم است که ناشی از تولید آنتیبادیهایی علیه کمپلکس فاکتور ۴ پلاکتی (PF4) و UFH میباشد. این آنتیبادیها میتوانند منجر به ترومبوز و ترومبوسیتوپنی شوند. در صورتی که HIT نوع ۲ مشکوک یا تأیید شود، باید از راهبردهای ضدانعقادی غیرهپارینی استفاده کرد. تشخیص HIT نوع ۲ باید در پرونده بیمار ثبت شود تا از تجویز هپارین لاک در پایان جلسات دیالیز جلوگیری شود. درمان این بیماران معمولاً تحت نظر متخصص خونشناسی انجام میشود.
ملاحظات ویژه برای دیالیز بیمارستانی
بیماران بستری با نارسایی حاد کلیه که نیاز به همودیالیز دارند:
معمولاً برای بیماران بستری که دیالیز حاد دریافت میکنند، از روش بدون هپارین استفاده میشود. اگر این بیماران دچار لختهشدگی مکرر در فیلتر دیالیز شوند، از پروتکل UFH یا هپارین با وزن مولکولی کم (LMWH) مشابه بیماران با ریسک استاندارد برای لخته شدن استفاده میشود.
بیماران بستری که تحت همودیالیز مزمن هستند
در بیمارانی که به دلیل بیماری کلیوی مرحله آخر (ESKD) به دیالیز مزمن وابسته هستند، در صورت بستری شدن در بیمارستان، معمولاً رژیم ضدانعقاد مشابه دیالیز سرپایی آنها ادامه مییابد. البته اگر این بیماران برای بررسی و مدیریت یک رویداد خونریزیدهنده بستری شده باشند یا قرار باشد تحت یک عمل جراحی بزرگ قرار گیرند، ریسک خونریزی او در طول بستری ارزیابی خواهد شد.
روشهایی که به ندرت برای ضدانعقاد در دیالیز استفاده میشوند
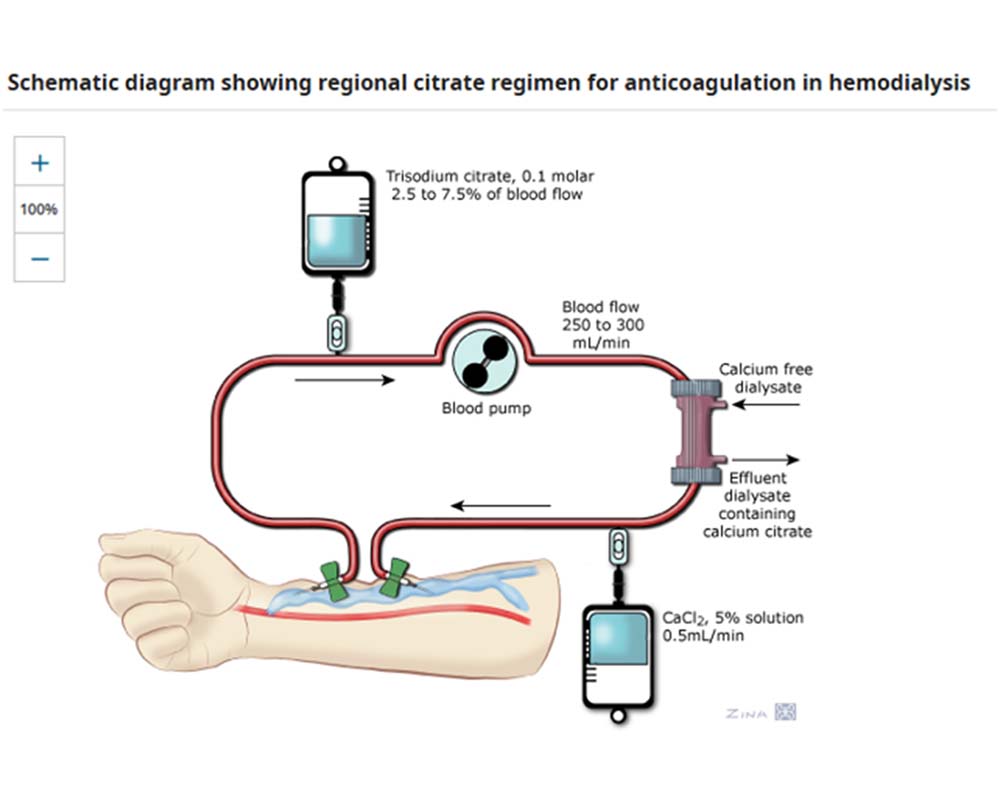
۱. ضدانعقاد منطقهای با سیترات (Regional Citrate Anticoagulation)
روشهایی که به ندرت برای ضدانعقاد در طی دیالیز استفاده میشوند شامل ضدانعقاد سیترات منطقهای است. در این روش، محلول سیترات تریسدیم ایزواسموتیک (با غلظت ۱۰۲ میلیمول در لیتر) بهصورت انفوزیون مداوم به شاخه شریانی صافی تزریق میشود. مکانیسم ضدانعقادی این روش به دلیل اتصال سیترات به کلسیم است که منجر به مهار آبشار انعقادی میشود.
در بیشتر مراکز از دیالیزات بدون کلسیم استفاده میشود و ضدانعقاد سیترات منطقهای را میتوان برای همودیالیز با فلاکس پایین و بالا و همچنین همودیافیلتراسیون به کار برد. غلظت سیترات ورودی به صافی در مراکز مختلف بین ۲.۷ تا ۴ میلیمول در لیتر متغیر است. با این حال، غلظتهای بالاتر تأثیری در بهبود هموکامپتیبیلیتی (سازگاری خون با دستگاه) نشان ندادهاند. برخی مطالعات نیز موفقیت دیالیز بدون استفاده از سیترات و تنها با دیالیزات بدون کلسیم و تزریق مجدد کلسیم را گزارش کردهاند. خنثیسازی اثر ضدانعقادی سیترات از طریق تزریق کلرید کلسیم ۵ درصد در مسیر بازگشت وریدی، با سرعت ۰.۵ میلیلیتر در دقیقه انجام میشود. این سرعت به طور مداوم تنظیم میشود تا از هایپوکلسمی (کاهش کلسیم خون) یا هایپرکلسمی (افزایش کلسیم خون) جلوگیری شود.
مطالعات مقایسهای نشان دادهاند که این روشها در مقایسه با پروتکلهای استاندارد هپارین غیرفرکشنه (UFH) باعث کاهش میزان خونریزی میشوند. مشکل اصلی ضدانعقاد سیترات منطقهای، هایپوکلسمی یا هایپرکلسمی، هایپرناترمی (به دلیل استفاده از محلول سیترات سدیم هیپرتونیک) و آلکالوز متابولیک (به دلیل تولید بیکربنات در طی متابولیسم سیترات) است که ممکن است نیاز به تزریق اسید هیدروکلریک داشته باشد. با این حال، در صورت مانیتورینگ دقیق، میزان عوارض نسبتاً پایین است. استفاده از دیالیزاتهای طراحیشده مخصوص ممکن است میزان اختلالات الکترولیتی از جمله آلکالوز متابولیک را کاهش دهد. میزان اثربخشی ضدانعقاد سیترات منطقهای در مراکز مختلف متفاوت است و میتواند تحت تأثیر نوع دسترسی عروقی، انتخاب صافی ، استفاده از همودیافیلتراسیون و عوامل مختلف بیمار قرار گیرد.
2.ضدانعقاد منطقهای با نافاموستات (Regional Anticoagulation with Nafamostat)
نافاموستات یک مهارکننده سرین پروتئاز است که عوارض جانبی افت فشار خون مرتبط با پروستاسیکلین را ندارد. این دارو عمدتاً به عنوان جایگزینی برای سیترات یا پروستاسیکلین در بعضی کشورهای آسیای شرقی استفاده میشود. نافاموستات نیمهعمر نسبتاً کوتاهی بین پنج تا هشت دقیقه دارد و نیازمند تزریق بولوس اولیه و سپس انفوزیون مداوم است که بر اساس زمان نسبی ترومبوپلاستین فعالشده (aPTT) تنظیم میشود.
مزیت اصلی این دارو این است که پس از رسیدن به هدف aPTT، دیگر نیازی به تنظیم دوز ندارد و به همین دلیل میتواند کنترل دقیقی را در بیمارانی که در معرض خطر بالای خونریزی هستند، فراهم کند. نافاموستات نباید با غشاهای دیالیز پلیآکریلونیتریل استفاده شود زیرا به سطح غشا جذب میشود.
اقدامات ایمنی برای کاهش خطاها و عفونت در واحدهای دیالیز
ا هپارین بهعنوان یک داروی با خطر بالا (High-Alert Medication) شناسایی شده که یکی از حوزههای تمرکز برای ایمنی بیماران است.
• هپارین غیرفرکشنه با دوز بالا و قدرت زیاد: محصولاتی که حاوی 50,000 واحد در هر ویال هستند (مانند 50000 واحد در 5 میلیلیتر یا 50000 واحد در 2 میلیلیتر) نباید در بخشهای ارائه خدمات به بیماران ذخیره شوند.
• هپارین غیرفرکشنه با دوز بالا: محصولات حاوی 10,000 واحد یا بیشتر در هر ویال (مانند 10000 واحد در 1 میلیلیتر، 10000 واحد در 10 میلیلیتر، یا 30000 واحد در 30 میلیلیتر) فقط باید در صورت نیاز و برای هر بیمار بهطور اختصاصی تجویز شوند.
• در شرایط خاص مراقبتی، ممکن است نیاز باشد که برخی محصولات هپارین در بخشهای خدمات بیماران موجود باشند. در چنین مواردی، کمیته بینرشتهای مدیریت داروها (مانند کمیته داروخانه و درمان و دبیرخانه مشورتی پزشکی)باید توجیه این تصمیم را بررسی و تأیید کند و تدابیر لازم را برای به حداقل رساندن خطرات ناشی از خطاهای دارویی اعمال نماید.
• ویالهای چند دوزی باید تا حد امکان فقط برای یک بیمار اختصاص داده شوند.
• اگر استفاده از ویالهای چند دوزی برای بیش از یک بیمار ضروری باشد، این ویالها باید فقط در یک منطقه اختصاصی برای آمادهسازی داروها (مانند ایستگاه پرستاری) نگهداری و استفاده شوند و از محیطهای درمانی مستقیم بیماران دور باشند.
• اگر یک ویال چند دوزی وارد منطقه درمان فوری بیمار شود، باید فقط برای استفاده یک بیمار اختصاص داده شود.
• ویالهای دارویی باید در صورت به خطر افتادن یا مشکوک بودن استریلیته، بلافاصله دور ریخته شوند.
• هر پرستار مسئول کشیدن هپارین در سرنگ برای بیماران خود است.
• دوزهای هپارین (هم بارگیری و هم انفوزیون مداوم) پس از تنظیم در دستگاه دیالیز، به بیمار تزریق میشود. ر تمام پرستاران آموزشهای تخصصی در مورد هپارین دریافت میکنند. این آموزشها شامل خطرات استفاده از هپارین بهعنوان یک داروی "High Alert" و اقدامات ایمنی مرتبط است.
• سرنگهای هپارین فقط در مناطق اختصاصی آمادهسازی دارو تهیه میشوند و ویالهای هپارین نباید وارد منطقه درمان بیمار شوند.
• سوزن/کانولا و سرنگ استفادهشده برای دسترسی به ویال چند دوزی باید استریل باشند.
• سوزن/کانولا و سرنگ هرگز مجدداً استفاده نمیشوند.
• ویالها قبل از وارد شدن سوزن/کانولا با الکل 70٪ ضدعفونی میشوند.
• در صورت به خطر افتادن یا مشکوک بودن استریلیته، ویالهای هپارین بلافاصله دور ریخته میشوند.
• اگر یک ویال چنددوزی وارد منطقه درمانی فوری بیمار شود، باید فقط برای استفاده یک بیمار اختصاص داده شود یا پس از استفاده دور انداخته شود.
• ویالهای چنددوزی هپارین که در پایان روز باقی میمانند، دور انداخته میشوند. در غیر این صورت، ممکن است حداکثر ۲۴ ساعت پس از باز شدن نگهداری شوند، به شرطی که تاریخ و زمان اولین ورود به ویال روی آن ثبت شده باشد. در هر صورت، واحدهای همودیالیز باید روی یک فرآیند برای پیگیری مدت زمان باز ماندن ویالها توافق کنند.
پروتامین سولفات
معمولاً زمانی که نیاز به خنثیسازی اثرات ضدانعقاد هپارین در بدن وجود داشته باشد، به ویژه در مواردی که خونریزی یا عوارض ناشی از هپارین بروز کرده باشد، از پروتامین سولفات استفاده میشود. در همودیالیز، هنگامی که هپارین برای جلوگیری از تشکیل لخته در دستگاه دیالیز و داخل شریانهای بیمار استفاده میشود، در پایان درمان دیالیز، ممکن است نیاز به پروتامین سولفات باشد تا اثرات ضد انعقاد هپارین را خنثی کرده و از خطرات خونریزی جلوگیری شود.
پروتامین سولفات با اتصال به هپارین، آن را بیاثر میکند و از ایجاد خونریزی ناخواسته جلوگیری مینماید. مقدار پروتامین سولفات باید با دقت و طبق دستور پزشک محاسبه شود، زیرا استفاده زیاد از آن خود میتواند منجر به ایجاد لختههای خون شود.
مکانیسم اثر:
پروتامین سولفات یک پروتئین قلیایی است که با هپارین ترکیب شده و یک کمپلکس پایدار و غیرفعال تشکیل میدهد، که باعث خنثی شدن اثرات ضدانعقادی هپارین میشود.
دوز و نحوه تجویز پروتامین سولفات برای خنثی کردن هپارین
دوز استاندارد:
o ۱ میلیگرم پروتامین سولفات برای خنثی کردن هر ۱۰۰ واحد هپارین سدیم که در ۲ تا ۳ ساعت گذشته تجویز شده باشد.
o حداکثر دوز توصیهشده در یک نوبت ۵۰ میلیگرم است.
محاسبه دوز بر اساس زمان مصرف هپارین:
o اگر از تزریق هپارین بیش از ۳۰ دقیقه گذشته باشد: دوز مورد نیاز را باید کاهش داد، زیرا هپارین بهتدریج متابولیزه شده است.
o اگر از تزریق هپارین بیش از ۲ ساعت گذشته باشد: معمولاً دوز پروتامین مورد نیاز کمتر از مقدار استاندارد است.
نحوه تجویز:
o پروتامین سولفات باید بهصورت وریدی (IV) و آهسته تزریق شود.
o سرعت تزریق نباید از ۵۰ میلیگرم در ۱۰ دقیقه تجاوز کند تا خطر بروز عوارض جانبی کاهش یابد.
عوارض جانبی احتمالی پروتامین سولفات:
• افت فشار خون
• برادیکاردی
• واکنشهای آلرژیک و آنافیلاکسی (بهخصوص در بیماران دیابتی تحت درمان با انسولین پروتامین)
• نارسایی قلبی یا مشکلات ریوی در برخی موارد
نکات مهم:
ش اگر بیمار دوزهای بالای هپارین دریافت کرده باشد، بهتر است پروتامین را بهصورت تقسیمشده و تدریجی تزریق کرد تا از بروز واکنشهای ناگهانی جلوگیری شود.
• تستهای انعقادی مانند ACT (Activated Clotting Time) یا aPTT (Activated Partial Thromboplastin Time) باید پس از تزریق پروتامین پایش شوند تا از خنثی شدن کافی هپارین اطمینان حاصل شود.
• برخی از ویالهای پروتامین سولفات، دوز را به جای میلیگرم (mg) بهصورت واحد بینالمللی (IU) نشان میدهند.
برای تبدیل و استفاده صحیح، مراحل زیر را در نظر بگیرید:
۱. رابطه بین میلیگرم و واحد بینالمللی (IU) پروتامین سولفات
• ۱ میلیگرم پروتامین سولفات تقریباً معادل ۱۰ واحد بینالمللی (IU) است.
۲. محاسبه دوز پروتامین سولفات برای خنثی کردن هپارین
• ۱ میلیگرم پروتامین سولفات برای خنثی کردن هر ۱۰۰ واحد هپارین استفاده میشود.
• بنابراین، ۱۰ IU پروتامین سولفات نیز میتواند ۱۰۰ واحد هپارین را خنثی کند.
۳. نحوه استفاده از ویالهای پروتامین سولفات
فرض کنید ویال شما ۵۰ میلیگرم/۵ میلیلیتر (یعنی ۱۰ میلیگرم در هر میلیلیتر) باشد. با توجه به اینکه هر ۱ میلیگرم = ۱۰ IU است، این ویال شامل ۵۰۰ IU در ۵ میلیلیتر (یعنی ۱۰۰ IU در هر میلیلیتر) خواهد بود.
۴. نکات مهم
• سرعت تزریق آهسته باشد (حداکثر ۵۰ میلیگرم در ۱۰ دقیقه)
• پایش انعقادی (ACT یا aPTT) انجام شود تا از خنثی شدن کافی هپارین اطمینان حاصل گردد.
• در صورت وجود خطر آلرژی یا واکنشهای حساسیتی، دوز را تدریجی و بهصورت تقسیمشده تزریق کنید.
آینده آنتی کواگولاسیون در دیالیز
پیشرفتهای اخیر در پزشکی منجر به توسعه داروهای ضدانعقادی جدیدی شده است که به کاهش خطرات خونریزی و بهبود کیفیت زندگی بیماران کمک میکند. مطالعات بر روی مهارکنندههای جدید فاکتور Xa و ترومبین نشان دادهاند که میتوانند جایگزین مناسبی برای روشهای سنتی باشند
داروهای ضد انعقاد نسل جدید
مهارکنندههای مستقیم ترومبین: مانند داپیگاتران، که پتانسیل کاهش نیاز به پایش مداوم را دارند.
مهارکنندههای فاکتور Xa: مانند ریواروکسابان و آپیکسابان که اثربخشی بالایی دارند و خطر خونریزی را کاهش میدهند.
روشهای نانوتکنولوژی: استفاده از سیستمهای تحویل هدفمند دارو برای بهینهسازی اثرات ضدانعقادی.
دیالیز بدون نیاز به آنتی کواگولانت؟
• توسعه فیلترهای جدید با سطوح ضدانعقادی که نیاز به داروهای ضدانعقاد را کاهش میدهند.
• استفاده از فناوریهای جدید مانند فیلترهای پوشش داده شده با پلیمرهای ضدانعقادی.
• با پیشرفتهای مداوم در این زمینه، آینده آنتی کواگولاسیون در دیالیز به سمت روشهای ایمنتر و کارآمدتر پیش خواهد رفت.
پرونده الکترونیک دیالیز (Diaysis Electronic Health Record - EHR) و سیستم دیاسیس چه نقشی در آنتیکواگولاسیون دارند؟
سیستمهای پرونده الکترونیک دیالیز مانند دیاسیس (Diaysis) به بهینهسازی مدیریت آنتیکواگولاسیون در بیماران دیالیزی کمک قابل توجهی میکنند. این سیستمها با ثبت دقیق دادههای بیمار، تجزیهوتحلیل اطلاعات و ارائه هشدارهای بالینی، تأثیر مثبتی بر کاهش عوارض ضدانعقادی دارند.
کمکهای کلیدی سیستم دیاسیس در آنتیکواگولاسیون دیالیز
1.پایش دقیق دوز و تنظیمات آنتیکواگولانتها
• ثبت مقدار هپارین یا سایر ضدانعقادهای مصرفی
• ارائه پیشنهادهای مبتنی بر الگوریتمهای هوشمند برای تنظیم دوز بر اساس وضعیت انعقادی بیمار
2.کاهش خطر عوارض جانبی (HIT، خونریزی و لخته شدن)
• هشدارهای خودکار در صورت افزایش یا کاهش بیش از حد دوز
• امکان مشاهده تاریخچه مصرف ضدانعقادها و تغییرات در هر جلسه دیالیز
3.یکپارچهسازی با نتایج آزمایشگاهی (PT، aPTT، INR)
• همگامسازی اطلاعات آزمایشات انعقادی با پروتکلهای درمانی
• تحلیل روند تغییرات پارامترهای انعقادی برای جلوگیری از خونریزی یا ترومبوز
4.افزایش ایمنی و شخصیسازی درمان بیماران
• پیشنهاد روشهای جایگزین برای بیماران با حساسیت به هپارین (مانند استفاده از سیترات)
• ایجاد پروتکلهای درمانی اختصاصی برای بیماران با ریسک بالای خونریزی
5.بهبود کارایی تیم درمانی
• دسترسی سریع به اطلاعات بیمار برای تصمیمگیری بهتر توسط پزشکان و پرستاران
• کاهش خطاهای انسانی در تجویز داروهای ضدانعقاد
نتیجه گیری
استفاده از ضد انعقادها در همودیالیز یکی از اجزای ضروری و حیاتی برای جلوگیری از تشکیل لختههای خونی در دستگاه دیالیز و درون شریانهای بیمار است. این فرآیند باعث حفظ جریان خون و بهبود کارایی درمان دیالیز میشود. انتخاب مناسب نوع ضد انعقاد، مقدار آن و زمان مصرف بر اساس وضعیت بالینی بیمار اهمیت فراوانی دارد. هپارین، یکی از رایجترین ضد انعقادهای مورد استفاده در همودیالیز است که باید با دقت و طبق دستور پزشک تنظیم شود. از طرفی، باید به عوارض احتمالی این داروها، مانند خونریزی، دقت کافی به عمل آید. همچنین استفاده از پرونده الکترونیک دیالیز (EHR) و سیستمهایی مانند دیاسیس میتواند نقش مهمی در بهبود ایمنی بیماران، کاهش عوارض آنتیکواگولاسیون و افزایش دقت در تنظیمات دارویی داشته باشد.
در مجموع، مدیریت دقیق و نظارت مستمر بر استفاده از ضد انعقادها میتواند به کاهش خطرات احتمالی کمک کند و تاثیر قابل توجهی در بهبود نتایج درمان دیالیز داشته باشد. پرستاران و پزشکان باید در این زمینه آموزشهای مناسب را دریافت کرده و از راهکارهای نوین برای بهینهسازی درمان استفاده کنند.
منابع مورد استفاده :
Handbook of dialysis(John T. Daugirdas )
Kidney Disease: Improving Global Outcomes (KDIGO)
چرا در همودیالیز نیاز به ضدانعقاد داریم؟
هنگامی که خون از مدار دیالیز عبور میکند، در تماس با سطوح خارجی قرار گرفته و سیستم انعقادی فعال میشود. برای جلوگیری از لخته شدن خون در مدار دیالیز و حفظ جریان خون مناسب، استفاده از داروهای ضدانعقاد ضروری است.
رایجترین داروی ضدانعقاد در همودیالیز چیست؟
هپارین غیرفرکشنه (UFH) رایجترین داروی ضدانعقادی در همودیالیز است. در اروپا، هپارین با وزن مولکولی پایین (LMWH) بیشتر مورد استفاده قرار میگیرد.
تفاوت هپارین غیرفرکشنه (UFH) و هپارین با وزن مولکولی پایین (LMWH) چیست؟
UFHنیمهعمر کوتاهتری دارد و نیاز به پایش مداوم دارد، اما اثر آن را میتوان با پروتامين سولفات معکوس کرد. LMWH اثر طولانیتر و پایدارتر دارد و نیاز به مانیتورینگ مداوم کمتری دارد.
چه زمانی از سیترات تریسدیم به جای هپارین استفاده میشود؟
سیترات تریسدیم در بیمارانی که خطر خونریزی بالایی دارند یا به هپارین حساسیت دارند، به عنوان جایگزین ضدانعقاد استفاده میشود.
در چه شرایطی نباید از ضدانعقاد استفاده کرد؟
در مواردی مانند خونریزی فعال، ترومبوسیتوپنی شدید، جراحی اخیر، خونریزی داخل جمجمهای و استفاده از داروهای ضدانعقادی سیستمیک، باید از ضدانعقاد اجتناب کرد.
چه عوارض جانبی رایجی در استفاده از هپارین وجود دارد؟
عوارض رایج شامل خونریزی، خارش، واکنشهای آلرژیک، پوکی استخوان، ریزش مو و ترومبوسیتوپنی است.
چگونه میتوان اثرات هپارین را معکوس کرد؟
در صورت بروز خونریزی بیش از حد، میتوان از پروتامين سولفات برای خنثی کردن اثرات هپارین استفاده کرد.
چگونه میتوان خطر خونریزی در بیماران دیالیزی را ارزیابی کرد؟
با بررسی سطح پلاکتها، وجود خونریزی فعال، جراحیهای اخیر و سابقه مصرف داروهای ضدانعقاد، میتوان خطر خونریزی بیمار را ارزیابی کرد.
دوز معمول هپارین در همودیالیز چقدر است؟
دوز اولیه معمولاً ۲۰۰۰ واحد است که از طریق لوله وریدی تزریق شده و پس از آن، تزریق مداوم با سرعت ۱۲۰۰ واحد در ساعت انجام میشود.
چه زمانی باید به جای UFH از داروهای جایگزین استفاده کرد؟
در بیمارانی که به هپارین حساسیت دارند، دچار ترومبوسیتوپنی ناشی از هپارین (HIT) هستند یا خطر خونریزی بالایی دارند، از داروهایی مانند آرگاتروبان، فونداپارینوکس یا نافاموستات مالئات استفاده میشود




